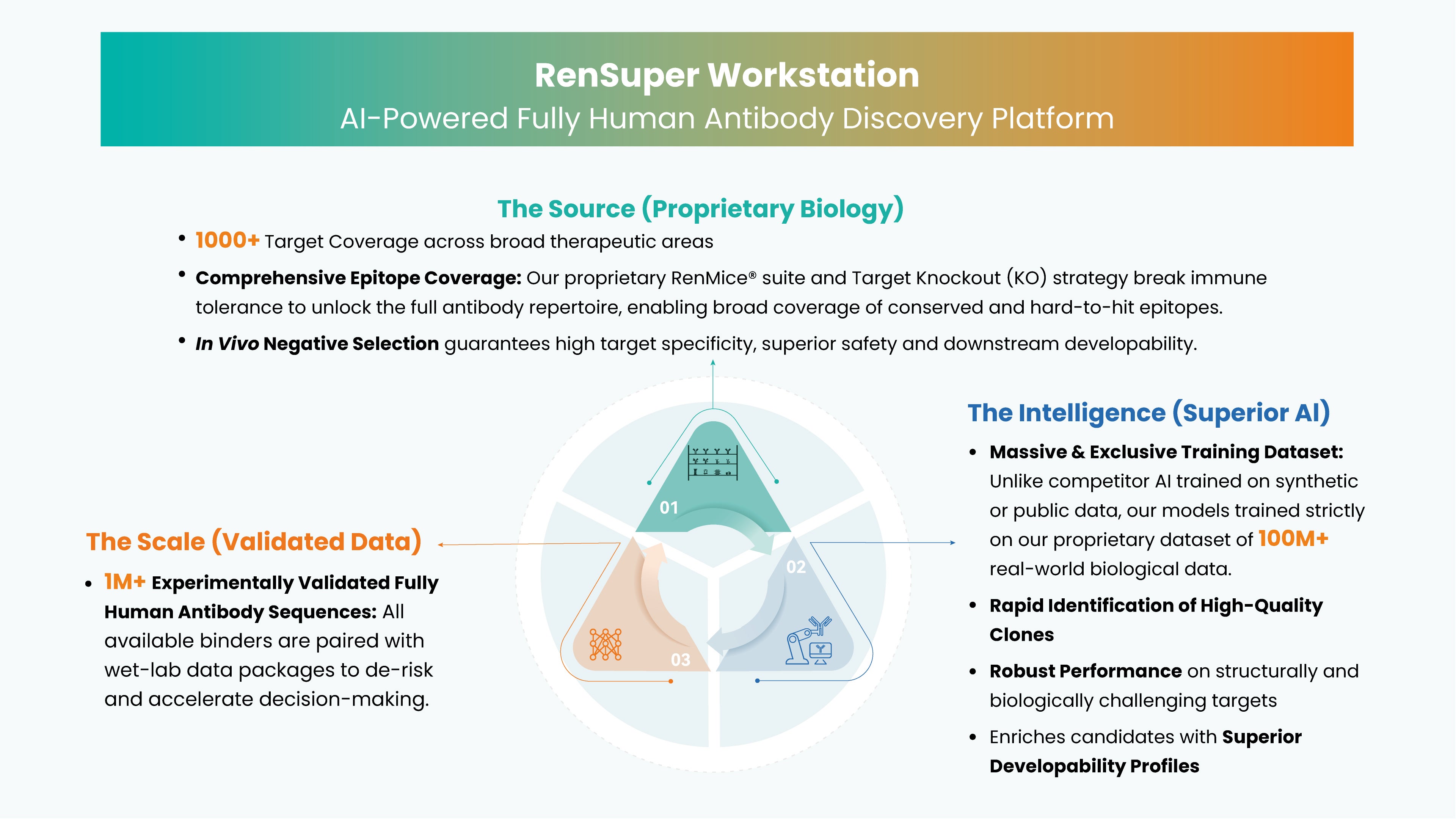
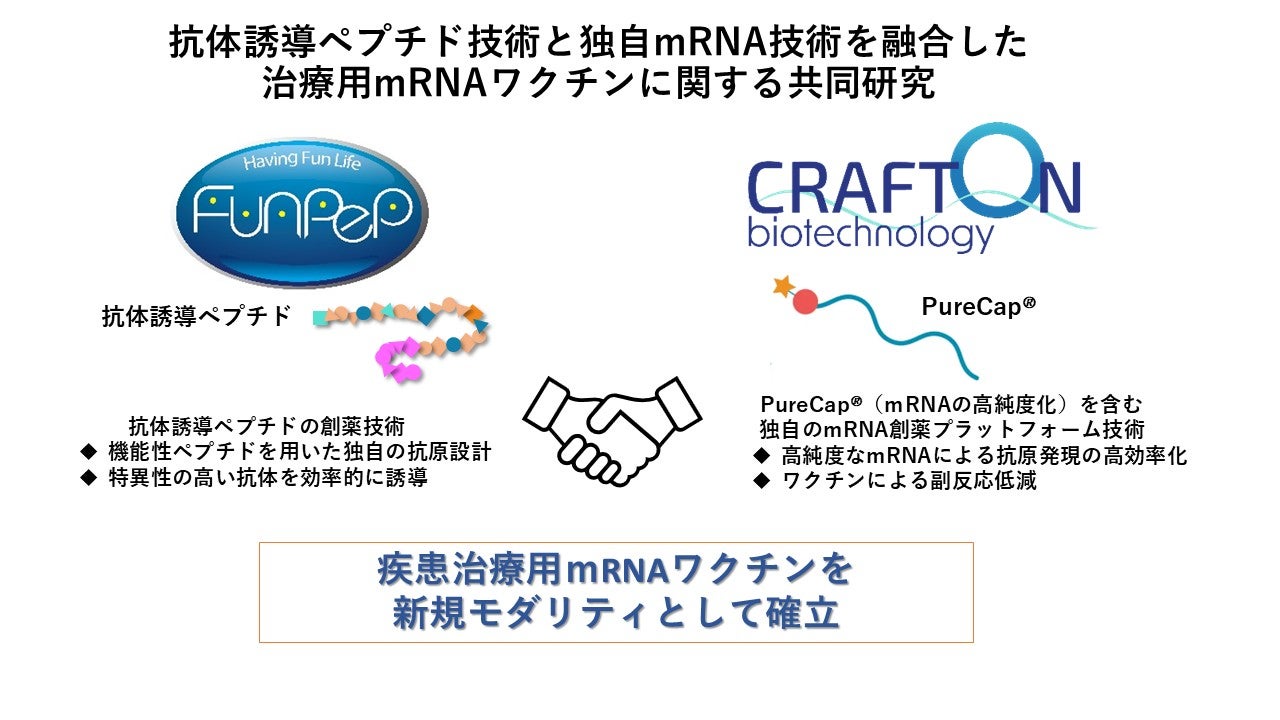
バイオ医薬品分野が急速に発展する中で、薬事戦略の策定、プロセス開発、技術移転の適切な進め方を理解することが成功の鍵となります。本ウェビナーでは、イノベーションを加速し、直面する課題を乗り越えるための実践的な知見をお届けします。また、バイオ医薬品開発を支援するための実践的な戦略についても議論します。
申込締切
2025年4月8日
プログラム
15:00-15:45
バイオ医薬品開発におけるCMC規制の考慮事項
- 薬品規制システムの概要(米国およびEU)
- 第I相臨床試験におけるCMC規制の考慮事項
- 臨床試験中の変更管理
- 後期開発段階(BLA/MAA)のCMC作業範囲
- 新薬の規制ライフサイクル管理に関するケーススタディ
15:45-16:30
複雑なバイオ医薬品のCMCにおける課題と解決策
以下の主要なCMCの課題に対する細胞株、細胞培養および精製開発戦略について議論します:
- 発現量の向上
- ホモ二量体生成の制御と除去
- アグリゲート生成の制御と除去
- N-グリカンの最適化
16:30-17:15
技術移転の強化:戦略、課題、およびベストプラクティス
- 技術移転のための効果的なアプローチ
- 技術移転における主要な課題と問題点
- ケーススタディの共有
- PPQにおける技術移転
主催
このウェビナーは、ジェンスクリプトジャパン株式会社とProBioが共催しています
お問い合わせ先
cdmo.jp@probiocdmo.com